一次看似不重的脑外伤,为何可能引发长期认知障碍,甚至增加神经退行性变化风险?创伤性脑损伤(TBI)发生后,大脑“应激信号”去甲肾上腺素(norepinephrine, NE)会迅速升高,这一点早已明确。但NE在细胞内部究竟从哪里开始“失控”,又如何把损伤逐级传递到线粒体并最终导致神经元死亡,长期缺少可直接观察的证据。
近日,华东师范大学田阳教授、刘智超研究员等团队设计出一种基于DNA纳米结构的化学遗传学纳米陷阱探针(NEtrap),实现对神经元细胞器内NE的动态成像与定量测量。研究首次在活细胞尺度实时捕捉到:TBI后内质网(ER)内出现NE快速“爆发”,并进一步串联起内质网应激、蛋白调控失衡、线粒体自噬增强与线粒体功能障碍等过程,勾勒出一条更清晰的神经元死亡路径。相关成果以Designing chemigenetic DNA nanotrap for norepinephrine dynamic imaging in organelles 为题发表于《Nature Chemical Biology》,并获得期刊“Research Briefing”关注。

神经递质识别是神经科学领域的前沿与难点,新神经递质的发现常常获得诺奖的青睐!但是因为神经递质的分子结构相似、且动态瞬时变化,如何获得神经递质的高选择性、快速识别,一直是具有挑战性的课题。田阳课题组历经六年攻关,取得系列重要进展:先后提出“双官能团顺序反应”、“多位点键合作用”等分子设计策略,实现去甲肾上腺素高选择性检测(Nat. Commun. 2023);基于“构象折叠”与“水桥”催化机制,将响应时间缩短至60毫秒(JACS 2023; JACS 2025);通过超分子识别体系实现谷氨酸、肾上腺素精准识别(JACS 2025; Nat. Commun. 2025)。然而,开发细胞器靶向的神经递质探针仍面临巨大挑战。
针对上述挑战,研究团队提出特异性化学反应识别和空间限域诱导的氢键/非共价作用多重协同识别策略,实现了神经元细胞器内NE的动态成像和定量检测。首先设计合成苯硼酸官能团的有机配体,利用其与儿茶酚胺邻苯二酚骨架发生特异性环化反应,实现初级识别;进一步构建框架核酸纳米结构,通过尺寸与构型的协同调控限域效应诱导氢键作用,放大不同儿茶酚胺与探针之间结合能垒差异,实现内质网中NE的高选择性定量分析。这种多重协同识别策略,还让NEtrap对NE的响应速度达到了前所未有的高度,快达50毫秒!这比现有的DNA适配体探针快了上万倍!
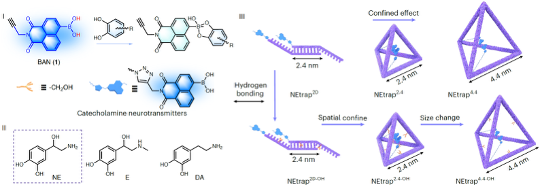
图1. NEtrap探针的结构示意图。
为了实现精准定量,团队还在探针上加装了一个“内置校准器”—荧光染料Cy3。当NE结合时,探针的主信号会减弱,而Cy3的参比信号保持不变,通过计算两者比值,就能排除环境干扰,得到绝对定量的NE浓度。此外,普通的化学探针在细胞内易扩散。为了解决这个问题,团队提出了“化学遗传学”(chemigenetic)的妙招。他们给NEtrap装上了一个叫HaloTag配体(HTL)的“锚”。只要在目标细胞器(如内质网、线粒体、细胞膜)的膜上表达对应的HaloTag蛋白,这个探针就能像“乐高积木”一样,共价、稳定地结合上去,一待就是48小时以上!这使得科学家们第一次能够长时间、高精度地测量不同细胞器内的NE水平。研究发现:细胞膜上的NE浓度约为92.9 nM;内质网(ER)中竟然也存在NE,浓度为32.8 nM—这是首次测到内质网中的NE基线水平!而线粒体内则几乎检测不到NE。
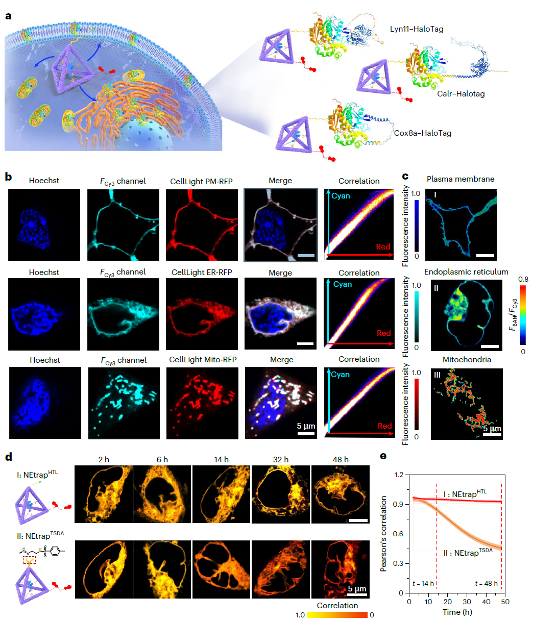
图2. NEtrap探针用于神经元不同细胞器中去甲肾上腺素的定量与成像分析
有了这个强大的工具,研究团队立刻将其应用于创伤性脑损伤(TBI)模型。结果令人震惊:在TBI发生后的0.6秒内,内质网中的NE浓度就开始急剧上升,并在60分钟内从约32 nM飙升至近190 nM!这是一个真正的“NE爆发”。更关键的是,这个内质网里的NE爆发,正是神经元死亡的“元凶”:触发内质网应激(ER Stress):NE的涌入激活了内质网的“压力警报”系统(GRP78蛋白水平大幅上升)。扰乱蛋白质调控内质网中的两种关键蛋白失衡——促代谢的Mthfd2上调,而保护线粒体的Nek1下调。引爆线粒体(Mitophagy):上述失衡信号传递到紧密相连的线粒体,导致促自噬蛋白Bnip3上调、呼吸链蛋白Uqcr11下调,最终引发大规模的线粒体自噬和功能障碍。神经元走向死亡整个过程形成一个恶性循环,最终导致神经元大量死亡。当研究人员用药物抑制NE的合成时,这一系列灾难性的连锁反应就被完全阻断,神经元存活率显著提高。这直接证明了内质网NE是TBI病理过程中的一个核心调控节点。
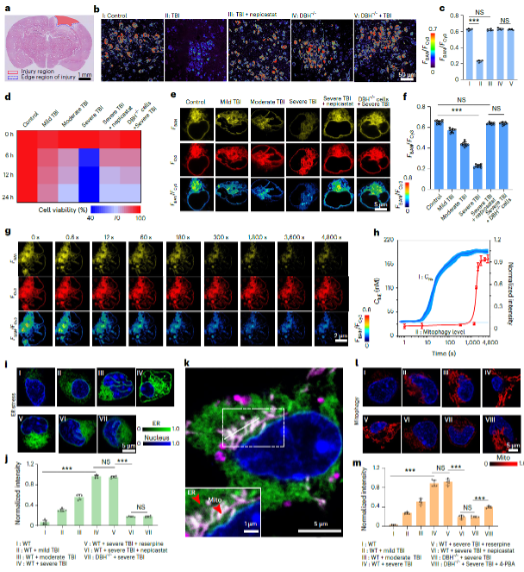
图3.神经元中TBI诱导的内质网应激过程中内质网中NE的实时成像与同步定量分析
这项研究的意义远不止于揭示了一个新机制。它所开发的NEtrap探针平台,为研究其他神经递质(如乙酰胆碱、谷氨酸)在细胞器内的动态提供了通用模板。更重要的是,它指明了内质网和NE信号通路可能是治疗TBI及相关疾病(如阿尔茨海默病、抑郁症、中风)的全新靶点。未来,或许能开发出专门清除内质网过量NE或阻断其下游信号的药物,为患者带来希望。论文第一作者为华东师范大学博士生陈奕林,论文的共同通讯作者为田阳教授和刘智超研究员。该研究得到了国家自然科学基金、国家重点研发计划、上海市科技创新行动计划基础研究项目等支持。
参考文献:Chen, Y., Liu, Z., Wang, Y. et al. Designing chemigenetic DNA nanotrap for norepinephrine dynamic imaging in organelles. Nat. Chem. Biol. (2026). https://doi.org/10.1038/s41589-026-02158-5.


 English
English

